|
ЙњМвЪГЦЗвЉЦЗМрЖНЙмРэзмОжгк2017Фъ3дТ28ШеЗЂВМЁЖвНгУЪфвКЁЂЪфбЊЁЂзЂЩфЦїОпгУШШЫмадОлАБѕЅзЈгУСЯЁЗЕФвНвЉаавЕБъзМЃЌВЂНЋгк2018Фъ4дТ1ШеЦ№е§ЪНЪЕЪЉЁЃ

БъзМдЮФШчЯТЃК
ЮяЕФЦЌМСЪЭвЉЛњжЦ
ЧАбд
БОБъзМАДееGB/T1.1-2009ИјГіЕФЙцЖЈЦ№ВнЁЃ
ЧызЂвтБОЮФМўЕФФГаЉФкШнПЩФмЩцМАзЈРћЁЃБОЮФЕФЗЂВМЛњЙЙВЛГаЕЃЪЖБ№етаЉзЈРћЕФд№ШЮЁЃ
БОБъзМгЩЙњМвЪГЦЗвЉЦЗМрЖНЙмРэзмОжЬсГіЁЃ
БОБъзМгЩШЋЙњвНгУЪфвКЦїОпБъзМЛЏММЪѕЮЏдБЛс(SAC/TC106)ЙщПкЁЃ
БОБъзМЦ№ВнЕЅЮЛЃКТЗВЉШѓЙмРэ(ЩЯКЃ)гаЯоЙЋЫОЁЂПЦЫМДДОлКЯЮя(жаЙњ)гаЯоЙЋЫОЁЂЩНЖЋЪЁвНСЦЦїаЕВњЦЗжЪСПМьбщжааФЁЃ
БОБъзМжївЊЦ№ВнШЫЃКАзБљЁЂБЁЯўЮФЁЂуЦИъЁЂРюКХЁЃ
гІгУТЗВЉШѓОлКЯЮяЕФЦЌМСЪЭвЉЛњжЦ
в§бд
вНгУШШЫмадОлАБѕЅОпгаСМКУЕФбгЩьадКЭПЙФгЧњадЃЌЧПЖШИпЁЂФЭФЅЫ№ЁЂЩњЮяЯрШнадСМКУЃЌЭЌЪБОлАБѕЅВФСЯОпгаЕФЮяРэЛњаЕадФмКЭМгЙЄадФмСМКУЃЌЪЙЦфдквНСЦСьгђЕУЕНЙуЗКгІгУЃЌШчОВТіСєжУеыЕФЬзЙмКЭбгГЄЙмЃЌЪфвКЦїЕФЕЮЖЗЁЂЕЮЙмЁЂЙмТЗЕШЁЃ
ЛљгкОлАБѕЅСЃСЯЕФКЯГЩЙЄвеЃЌСЃСЯжаПЩФмДцдкВаСєЕФЖўвьЧшЫсѕЅРрЕЅЬхЁЃдкЦфМгЙЄЙ§ГЬжавргаПЩФмВњЩњИУРрЕЅЬхЁЃгаЮФЯзБЈЕРВаСєЕЅЬхМАЦфЫЎНтВњЮяОпгавЛЖЈЖОадЁЃ
е§ЮФФкШн
1.ЗЖЮЇ
БОБъзМЙцЖЈСЫвНгУЪфвКЁЂЪфбЊЁЂзЂЩфЦїОпгУШШЫмадОлАБѕЅзЈгУСЯ(TPU)(вдЯТМђГЦОлАБѕЅзЈгУСЯ)ЕФММЪѕвЊЧѓМАЪдбщЗНЗЈЁЂБъжОЁЂАќзАКЭжќДцЁЃ
БОБъзМжЛЪЪгУгкзщЗжЕЅвЛЕФОлАБѕЅзЈгУСЯЃЌВЛЪЪгУгкЙВЛьОлАБѕЅзЈгУСЯ(ШчОлАБѕЅ/ОлТШввЯЉЁЂОлАБѕЅ/ОлМзШЉЕШ)МАЬэМгЦфЫћГЩЗж(ШчЯдгАМСЃЌзХЩЋМСЁЂВЃСЇЯЫЮЌЕШ)ЕФОлАБѕЅзЈгУСЯЁЃ
гІгУТЗВЉШѓОлКЯЮяЕФЦЌМСЪЭвЉЛњжЦ
2.ЙцЗЖадв§гУЮФМў
ЯТСаЮФМўЖдгкБОЮФМўЕФгІгУЪЧБиВЛПЩЩйЕФЁЃЗВЪЧзЂШеЦкЕФв§гУЮФМўЃЌНізЂШеЦкЕФАцБОЪЪгУгкБОЮФМўЁЃЗВЪЧВЛзЂШеЦкЕФв§гУЮФМўЃЌЦфзюаТАцБО(АќРЈЫљгаЕФаоИФЕЅ)ЪЪгУгкБОЮФМўЁЃ
GB/T528-2009СђЛЏЯ№НКЛђШШЫмадЯ№НКРЩьгІСІгІБфадФмЕФВтЖЈ
GB/T529-2008СђЛЏЯ№НКЛђШШЫмадЯ№НКЫКСбЧПЖШЕФВтЖЈ(ПуаЮЁЂжБНЧаЮКЭаТдТаЮЪдбљ)
GB/T1040.1-2006ЫмСЯРЩьадФмЕФВтЖЈЕк1ВПЗжЃКзмдђ
GB/T2411-2008ЫмСЯКЭгВЯ№НКЪЙгУгВЖШМЦВтЖЈбЙКлгВЖШ(ЩлЪЯгВЖШ)
GB/T2918-1998ЫмСЯЪдбљзДЬЌЕїНкКЭЪдбщЕФБъзМЛЗОГ
GB/T3398.2-2008ЫмСЯгВЖШВтЪдЕкЖўВПЗжЃКТхЪЯгВЖШ
GB/T6682-2008ЗжЮіЪЕбщЪвгУЫЎЙцИёКЭЪдбщЗНЗЈ
GB/T9352-2008ЫмСЯШШЫмадВФСЯЪдбљЕФбЙЫм
GB/T14233.1-2008вНгУЪфвКЁЂЪфбЊЁЂзЂЩфЦїОпЕк1ВПЗжЃКЛЏбЇЗжЮіЗЈ
GB/T16886.1вНСЦЦїаЕЩњЮябЇЦРМлЕк1ВПЗжЃКЦРМлгыЪдбщ
GB/T17037.1-1997ШШЫмадЫмСЯВФСЯзЂЫмЪдбљЕФжЦБИЕк1ВПЗжЃКвЛАудРэМАЖргУЭОЪдбљКЭГЄЬѕЪдбљЕФжЦБИ
жаЛЊШЫУёЙВКЭЙњвЉЕф(2015АцЫФВП)
3.вЊЧѓ
3.1МјБ№
АДжаЛЊШЫУёЙВКЭЙњвЉЕф2015АцЫФВП0402КьЭтЗжЙтЙтЖШЗЈНјааВтЖЈЃЌвНгУОлАБѕЅзЈгУСЯКьЭтЭМЦзгІгыжЦдьЩЬЬсЙЉЕФЭМЦзвЛжТЁЃ
3.2ЭтЙл
АД4.3НјааЪдбщЃЌвНгУОлАБѕЅзЈгУСЯЮЊОљдШПХСЃЃЌЮоЭтРДдгжЪЁЃ
3.3ЮяРэадФм
вНгУОлАБѕЅзЈгУСЯЕФЮяРэадФмгІЗћКЯБэ1ЕФЙцЖЈЁЃ
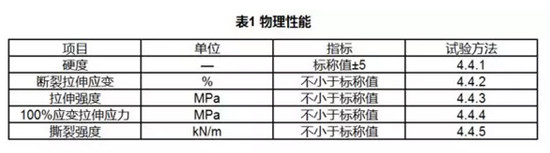
3.4ЛЏбЇадФм
вНгУОлАБѕЅзЈгУСЯЕФЛЏбЇадФмгІЗћКЯБэ2ЕФЙцЖЈ
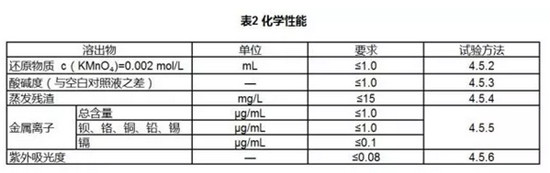
3.5ЩњЮяЯрШнад
GB/T16886.1ЖдвНгУОлАБѕЅзЈгУСЯНјааЩњЮябЇЦРМлЪБЃЌЦРМлНсЙћгІБэУїЮоВЛПЩНгЪмЕФЩњЮябЇЮЃКІЁЃ
зЂЃКGB/T14233.2ЙцЖЈЕФЩњЮябЇЪдбщЗНЗЈгІШЯЮЊЪЧGB/T16886жаЙцЖЈЕФЗНЗЈЕФВЙГфЁЃЩњЮябЇЦРМлвЫЛљгкВФСЯдЄЦкжЦдьЦїаЕЕФОпЬхЧщПіКЭЫљОЪмЕФУ№ОњЙ§ГЬЁЃ
4.ЪдбщЗНЗЈ
4.1ЪдбљЕФжЦБИ
ЮяРэадФмЕФВтЪдВЩгУбЙЫмЪдЦЌЃЌЦфжЦБИАДGB/T9352-2008ЕФЙцЖЈЁЃЩњЮябЇЦРМлвВПЩВЩгУзЂЫмЪдЦЌЃЌЦфжЦБИАДGB/T17037.1-1997ЕФЙцЖЈЁЃ
зЂЃКЮЊСЫЪЙЪдбщНсЙћФмДњБэзюжеЦїаЕЕФадФмЃЌЪдЦЌжЦБИКѓПЩЪЙЦфОЪмвНСЦЦїаЕдЄЦкЕФУ№ОњЙ§ГЬЁЃ
гІгУТЗВЉШѓОлКЯЮяЕФЦЌМСЪЭвЉЛњжЦ
4.2ЪдбљЕФзДЬЌЕїНкКЭЪдбщЕФБъзМЛЗОГ
ЪдбљЕФзДЬЌЕїНкАДGB/T2918-1998ЕФЙцЖЈНјааЃЌзДЬЌЕїНкЕФЬѕМўЮЊ2МЖБъзМЛЗОГ(23/50),ЕїНкЪБМфжСЩй40hЃЌЕЋВЛГЌЙ§96hЁЃ
4.3ЭтЙл
дкздШЛЙтЯпЛђШеЙтЕЦЯТЃЌгУе§ГЃЪгСІЛђНУе§ЪгСІЙлВьЁЃ
4.4ЮяРэадФм
4.4.1гВЖШ
ЖдБъГЦгВЖШаЁгк85DЕФзЈгУСЯЃЌШЁЪдЦЌАДGB/T2411-2008НјааЪдбщЁЃгВЖШМЦВЩгУЩлЪЯAЃЌЪЉМгИККЩ1.00kg�0.01kg,ЕБAаЭгВЖШМЦЕФЪОжЕДѓгк90ЪБЃЌВЩгУDаЭгВЖШМЦЃЌЪЉМгИККЩ5.00kg�0.01kgЁЃЖдБъГЦгВЖШДѓгк100DЕФзЈгУСЯЃЌШЁЪдЦЌАДGB/T3398.2-2008НјааЪдбщЁЃЪдбщЕуВЛЕУаЁгк5ИіЁЃ
4.4.2ЖЯСбРЩьгІБф
АД4.1жЦБИЪдЦЌЃЌЪдЦЌАД4.2ЙцЖЈНјаазДЬЌЕїНкЁЃ
ШЁЕїНкЕФЪдЦЌЃЌАДGB/T528-2009жа1аЭЪдбљжЦБИбљЦЌЃЌАДGB/T1040.1-2006НјааЪдбщЃЌЪдбщЫйЖШ200mm/minЁЃ
4.4.3РЩьЧПЖШ
АД4.1жЦБИЪдЦЌЃЌЪдЦЌАД4.2ЙцЖЈНјаазДЬЌЕїНкЁЃ
ШЁЕїНкЕФЪдЦЌЃЌАДGB/T528-2009жа1аЭЪдбљВУШЁбљЦЌЃЌАДGB/T1040.1-2006НјааЪдбщЃЌЪдбщЫйЖШ200mm/minЁЃ
4.4.4100%гІБфРЩьгІСІ
АД4.1жЦБИЪдЦЌЃЌЪдЦЌАД4.2ЙцЖЈНјаазДЬЌЕїНкЁЃ
ШЁЕїНкЕФЪдЦЌЃЌАДGB/T528-2009жа1аЭЪдбљВУШЁбљЦЌЃЌАДGB/T1040.1-2006НјааЪдбщЃЌЪдбщЫйЖШ200mm/minЁЃ
4.4.5ЫКСбЧПЖШ
АД4.1жЦБИЪдЦЌЃЌЪдЦЌАД4.2ЙцЖЈНјаазДЬЌЕїНкЁЃ
ШЁЕїНкЕФЪдЦЌЃЌАДGB/T529-2008жажБНЧаЮЮоШБПкЪдбљВУШЁбљЦЌЃЌАДGB/T529-2008НјааЪдбщЃЌЪдбщЫйЖШ500mm/minЁЃ
4.5ШмГіЮяЛЏбЇадФм
4.5.1ЙЉЪдвКжЦБИ
ГЦШЁСЃСЯЃЌгУЗћКЯGB/T6682-2008ЙцЖЈЕФЖўМЖЪдбщгУЫЎГхЯДИЩОЛЃЌАДжЪСП(g)гыЫЎ(mL)БШЮЊ1ЃК5ЕФБШР§МгЫЎЃЌ37Ёц�1ЁцЬѕМўЯТЃЌНўЬс72hЃЌНЋбљЦЗгывКЬхЗжРыЃЌРфШДжСЪвЮТМДЕУЁЃШЁЭЌХњЫЎвдЭЌЗЈжЦБИПеАзЖдБШвКЁЃ
4.5.2ЛЙдЮяжЪ
ШЁЕУ4.5.1жЦБИЕФЙЉЪдвККЭЖдеевКЃЌАДGB/T14233.1-2008жа5.2.2НјааЪдбщЁЃ
4.5.3ЫсМюЖШ
ШЁЕУ4.5.1жЦБИЕФЙЉЪдвККЭЖдеевКЃЌАДGB/T14233.1-2008жа5.4.1НјааЪдбщЁЃ
4.5.4еєЗЂВадќ
ШЁАД4.5.1жЦБИЕФЙЉЪдвККЭЖдеевКЃЌАДGB/T14233.1-2008жа5.5НјааЪдбщЁЃ
4.5.5Н№ЪєРызг
ШЁАД4.5.1жЦБИЕФЙЉЪдвКЃЌАДGB/T14233.1-2008жа5.6.1КЭ/ЛђдзгЮќЪеЗжЙтЙтЖШЗЈ(AAS)ЛђЯрЕБЕФЗНЗЈНјааЪдбщЁЃ
4.5.6зЯЭтЮќЙтЖШ
ШЁАД4.5.1жЦБИЕФЙЉЪдвКЃЌАДGB/T14233.1-2008жа5.7ЙцЖЈдк220nm-350nmВЈГЄЗЖЮЇФкНјааЪдбщЁЃ
5БъжО
вНгУОлАБѕЅзЈгУСЯВњЦЗЭтАќзАДќЩЯЕФБъжОгІАќРЈЯТСаФкШн:
a)ВњЦЗУћГЦ;
b)ГЇЩЬУћГЦЛђЩЬБъ;
c)аЭКХ;
d)ХњКХ;
e)ОЛжиЁЃ
6АќзАЁЂжќДц
6.1АќзА
вНгУОлАБѕЅзЈгУСЯгІжСЩйВЩгУЫЋВуАќзАЃЌАќзАгІБЃжЄдкВњЦЗдЫЪфЁЂжќДцЪБВЛБЛЮлШОЁЃ
6.2жќДц
вНгУОлАБѕЅзЈгУСЯгІжќДцдкЭЈЗчЁЂИЩдяЁЂЧхНрВЂБЃГжгаСМКУЯћЗРЩшЪЉЕФВжПтФкЁЃжќДцЪБдЖРыШШдДЃЌВЂЗРжЙбєЙтжБЩфЁЃ
|

